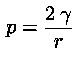Le lamine liquide sono contrattili ed assumono la superficie minima
compatibilmente con i vincoli e le forze esterne applicate, cioè
l'energia potenziale superficiale relativa alla configurazione di
equilibrio è, come nel caso della meccanica, minima.
L'allargamento di un liquido su un altro o il raccogliersi in gocce sono
conseguenze della ricerca della configurazione di minore energia
superficiale. Prendiamo il caso della superficie di separazione
liquido-vuoto. La molecola di liquido è sottoposta all'azione
attrattiva delle molecole circostanti, azione che diminuisce rapidamente
con la distanza e si può ritenere sostanzialmente nulla ad una
distanza r (100 - 1000 volte più grande del raggio molecolare)
dipendente dal tipo di molecola ma comunque dell'ordine di grandezza del
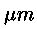 , detto raggio della sfera d'azione molecolare.
, detto raggio della sfera d'azione molecolare.
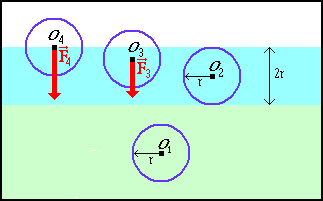
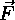 ed è crescente man mano che la molecola si avvicina alla superficie
del liquido.
ed è crescente man mano che la molecola si avvicina alla superficie
del liquido.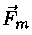 ( forza media di coesione ) per un tratto r ( raggio d'azione ).
Il lavoro che serve ad aumentare la superficie di 1 cm² sarà
circa :
( forza media di coesione ) per un tratto r ( raggio d'azione ).
Il lavoro che serve ad aumentare la superficie di 1 cm² sarà
circa :
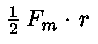
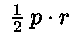
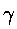 il lavoro per unità di superficie si ha
il lavoro per unità di superficie si ha